如何准确判断电离程度的大小?
在化学学习中,电离程度是一个重要的概念,它描述了分子或原子失去或获取电子形成离子的能力。了解电离程度的大小对于判断物质的性质、反应活性以及在实际应用中的表现至关重要。那么,电离程度大小究竟怎么判断呢?以下将从多个方面详细介绍。

一、电离能与电离度的基本概念
电离程度指的是分子或原子从中丧失或获取一个或多个电子形成离子的能力,通常用电离能或电离度来表示。电离能是将一个电子从一个原子或分子的基态中移除所需的最小能量。电离能越小,说明一个原子或分子失去电子的能力越强,即其电离程度越大。电离度则是衡量电解质在溶液中电离程度的指标,其计算公式为电离度α =(已电离的电解质分子数 / 原电解质分子数)× 100%。
二、查找电离能数值
要判断一个物质的电离程度大小,最直接的方法之一是查找相关资料或参考书籍,了解物质的电离能数值。一般来说,电离能越小的物质其电离程度越大。电离能数据可以通过专业数据库或化学手册获取。例如,金属元素的电离能通常较低,因此它们较容易失去电子形成离子。
三、观察物质在电场中的表现
电场中的物质表现出的电离效应也可以帮助我们判断其电离程度。电离程度大的物质在电场中会表现出更强的电离效应,比如发出明亮的光或者形成等离子体等。这是因为电场作用会使物质中的电子更容易被移除,形成离子。
四、测量物质的导电性
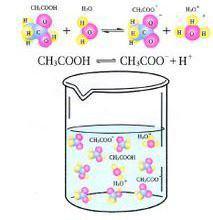
导电性是判断物质电离程度的另一个重要指标。电离程度高的物质会表现出更好的导电性能,因为其在水溶液或者气态环境中会释放出更多的离子,从而增加了电导率。例如,强电解质如盐类(NaCl)在水中会完全电离,形成大量的Na+和Cl-离子,因此具有良好的导电性。而弱电解质如醋酸(CH3COOH)则只能部分电离,导电性相对较差。
五、电离常数
对于弱电解质,电离常数是衡量其电离能力的一个重要指标。电离常数越大,说明电解质的电离能力越强。例如,醋酸(CH3COOH)和一水合氨(NH3·H2O)虽然都是弱电解质,但它们的电离常数较大,因此电离程度较大。电离常数可以通过实验测定,也可以通过查阅相关文献获取。
六、溶液的pH值与离子浓度
对于酸性或碱性溶液,电离程度越高,pH值越偏离7。例如,强酸如硫酸(H2SO4)和盐酸(HCl)会完全电离,pH值会远低于7。而弱酸如醋酸则只能部分电离,pH值相对接近7。此外,通过仪器测量溶液中离子的浓度,可以更准确地判断电离程度。强电解质在溶液中会完全电离,所以离子浓度高;而弱电解质只部分电离,所以离子浓度相对较低。
七、温度与电离程度
温度是影响电离程度的一个重要因素。一般来说,温度越高,电离程度越大。这是因为电离过程是一个吸热过程,温度升高可以增大电离度。然而,需要注意的是,对于某些特定的物质,如水的电离,温度的影响可能更为显著。随着温度的升高,水的电离程度会增大,因为高温有助于克服电离所需的能量障碍。
八、溶质的性质与电离程度
溶质的性质也会影响溶液的电离程度。例如,加入酸、碱会抑制水的电离,因为酸碱中和反应会消耗一部分H+或OH-,从而降低水的电离度。相反,加入弱酸强碱盐或强碱弱酸盐会加强水的电离。这是因为这些盐在水中电离产生的离子会与水分子发生反应,促进水的电离。
九、常见酸的电离程度比较
通过比较常见酸的电离程度,也可以对物质的电离程度有一个大致的了解。例如,HIO3的电离度相对较高,而HS-的电离度则非常低。这是因为不同酸的电离能力不同,酸性越弱表明电离程度越低。常见不完全电离的酸排序(以一级电离为准)为:HIO3 > H2CO4 > H2SO3 > HSO4- > H3PO4 > HNO2 > HF > HC2O4- > HAc > H2CO3 > HSO3- > H2PO4- > H2S > HClO > HCN > HCO3- > HPO4^2- > HS-。越靠前的酸电离度越大。
十、实际应用中的综合考虑
在实际应用中,判断物质的电离程度大小需要综合考虑多种因素。除了上述提到的电离能、导电性、电离常数、pH值、离子浓度、温度、溶质性质等外,还需要考虑物质的浓度、压力以及化学环境等因素。例如,在高压条件下,某些物质的电离程度可能会发生变化。此外,不同的化学环境也可能对物质的电离程度产生影响。
十一、电离度的应用实例
电离
- 上一篇: KDJ指标结合布林带微交易策略实战步骤
- 下一篇: 如何找回QQ号登录密码
-
 电离度的计算公式是什么?资讯攻略11-01
电离度的计算公式是什么?资讯攻略11-01 -
 如何判断咖啡生豆的新鲜程度资讯攻略11-14
如何判断咖啡生豆的新鲜程度资讯攻略11-14 -

-
 强酸制备弱酸的原理及实例资讯攻略03-05
强酸制备弱酸的原理及实例资讯攻略03-05 -
 揭秘:如何准确判断“几点钟方向”?资讯攻略12-07
揭秘:如何准确判断“几点钟方向”?资讯攻略12-07 -
 如何准确描述树的特征资讯攻略10-31
如何准确描述树的特征资讯攻略10-31












